Kimya Laboratuvarlarında Kullanılan Bazı Teknikler
Videolar
DEKANTASYON
Bir sıvının dibine çökmüş olan katılar ayrılmak istenirse, sıvı yavaş yavaş başka bir kaba aktarılır. Böylece dipteki katı madde kapta kalır. Bu ayırma yöntemine dekantasyon denir. Dekantasyon işlemi sıvı-sıvı heterojen karışımların ayrılmasında da kullanılır.
DESTİLASYON (DAMITMA)
Sıvı karışımların birbirlerinden ayrılması için uygulanan temel yöntem damıtma yöntemidir. Bu yöntemin temeli ise, sıvıları kaynama noktaları arasındaki farklardan yararlanılarak birbirlerinden ayırmaktır. Bu kaynama noktaları farklarının az veya çok olmasına göre damıtma yöntemi birkaç çeşide ayrılmaktadır.
Basit Destilasyon :
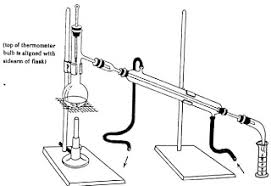 Kaynama noktaları arasındaki farkları çok fazla olan sıvıları birbirinden ayırmada kullanılır.
Kaynama noktaları arasındaki farkları çok fazla olan sıvıları birbirinden ayırmada kullanılır.
Ayrımsal Destilasyon :
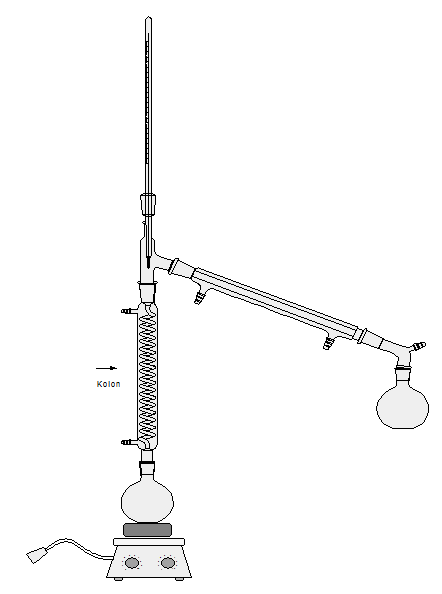 Sıvı karışımları arasındaki kaynama noktası farkı çok küçükse ayırma ve saflaştırma işlemi olarak bu yöntem uygulanır. Bu sistemin sanayide uygulama alanı da Petrol sanayisidir. Sabit kaynama noktasına sahip olan karışımlara azeotropik karışımlar denir. Bu karışımdaki bileşenleri birbirinden ayırmak için ayrımsal damıtma sistemi uygulanır. Ayrımsal damıtma sonunda bazı kirlilik ve renklilik oluşabilir. Bunu gidermek için son olarak basit damıtma uygulanmalıdır.
Sıvı karışımları arasındaki kaynama noktası farkı çok küçükse ayırma ve saflaştırma işlemi olarak bu yöntem uygulanır. Bu sistemin sanayide uygulama alanı da Petrol sanayisidir. Sabit kaynama noktasına sahip olan karışımlara azeotropik karışımlar denir. Bu karışımdaki bileşenleri birbirinden ayırmak için ayrımsal damıtma sistemi uygulanır. Ayrımsal damıtma sonunda bazı kirlilik ve renklilik oluşabilir. Bunu gidermek için son olarak basit damıtma uygulanmalıdır.
Düşük Basınç Altında Destilasyonu (Vakum Damıtması) :
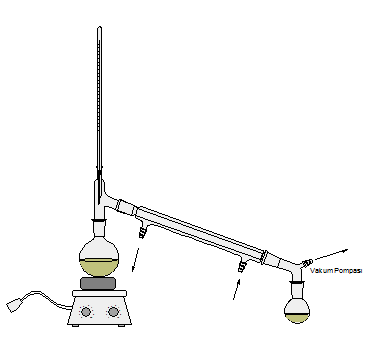 Kendi kaynama noktasına gelmeden bozunan ve kaynama noktası çok yüksek olan bileşikleri bozunmadan elde edebilmek için uygulanan işlemdir. Burada düşük basınç uygulamak için kullanılan malzeme vakum pompası ve su trompudur. Bir sıvı ısıtıldığında buhar basıncı dış basınca eşit olunca kaynama başlar. Bu sebeple damıtma sisteminde dış basınç düşürüldüğü takdirde bileşiğin daha düşük bir sıcaklıkta kaynayarak damıtılması sağlanır.
Kendi kaynama noktasına gelmeden bozunan ve kaynama noktası çok yüksek olan bileşikleri bozunmadan elde edebilmek için uygulanan işlemdir. Burada düşük basınç uygulamak için kullanılan malzeme vakum pompası ve su trompudur. Bir sıvı ısıtıldığında buhar basıncı dış basınca eşit olunca kaynama başlar. Bu sebeple damıtma sisteminde dış basınç düşürüldüğü takdirde bileşiğin daha düşük bir sıcaklıkta kaynayarak damıtılması sağlanır.
Su Buharı Destilasyonu :
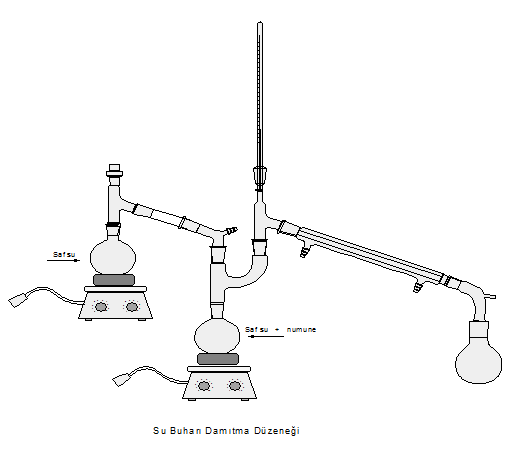 Suda çözünmeyen ve miktarı az olan maddeleri uçucu olmayan karışımlardan ayırmak için özellikle madde 100 oC nin üzerinde kaynıyorsa ve kaynama noktasına yakın sıcaklıklarda bozunuyorsa su buharı destilasyonu kullanılır.
Suda çözünmeyen ve miktarı az olan maddeleri uçucu olmayan karışımlardan ayırmak için özellikle madde 100 oC nin üzerinde kaynıyorsa ve kaynama noktasına yakın sıcaklıklarda bozunuyorsa su buharı destilasyonu kullanılır.
KİMYASALLARI KOKLAMAK
SÜZME İŞLEMİ
SU TROMPUNU KULLANMAK
TERAZİ KULLANIMI